スペクトル
スペクトルは,光の中に含まれる波長を表したものです.
光をプリズムに入れて光が分かれる時の様子のことでもあります.
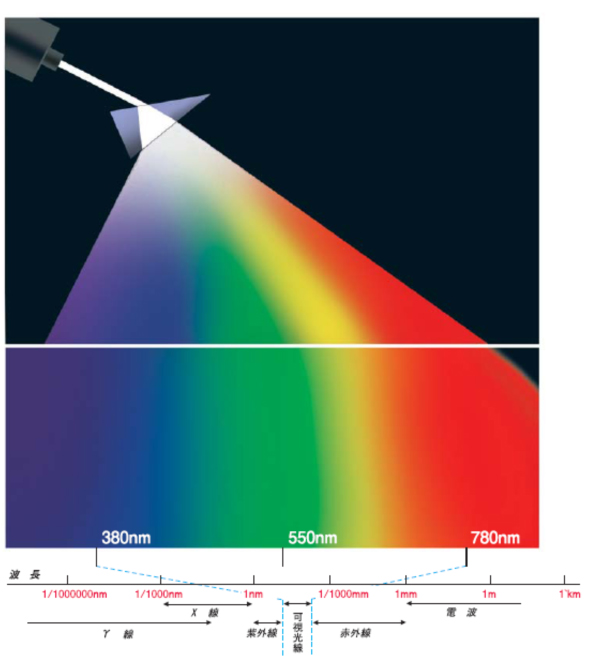
画像は日本電色工業様の物を使用させていただいております.https://www.nippondenshoku.co.jp/web/japanese/colorstory/05_spectrum.htm
こんな感じで虹のような状態が出来上がります.これがスペクトル.
連続スペクトルと線スペクトル
まずは連続スペクトルの画像から.

切れ目がないなめらかなグラデーションになっているものが連続スペクトル.これはイメージしやすいですよね?
それに対して,ちょっと直観的にはイメージしづらいのが線スペクトル↓

こんな感じで飛び飛びの波長だけ現れるのが線スペクトル.
線スペクトルは,気体が高い温度に熱されたときに放つ特有のスペクトルで,気体ごとに放出するスペクトルは決まっています.
いろんなところで使用されている水銀灯なんかも,実はこのスペクトルの光しか出ていません.このスペクトルが混ざることによって,私たちは「白っぽい明りだなぁ」と感じているわけです.
逆に,気体に光が当たると,その気体特有の線スペクトルの波長だけ吸い取られたスペクトルが観測されます.
線スペクトルができる理由(ある程度分かる人向け)
エネルギー準位?なにそれおいしいの?って人は次の章を見てください.
線スペクトルは,励起状態の電子がエネルギー準位の低い状態に移るときに余ったエネルギーを光として放出することで起きる現象です.
エネルギー準位は原子によって複数の決まった値を持つので,余ったエネルギーも複数の決まった値を持つ.つまり,発生する光も複数の決まった値を持つわけです.
光のエネルギー
$$E=hν=\frac{hc}{λ}$$
\(h\):プランク定数
\(ν\):振動数
\(λ\):波長
基底状態と励起状態
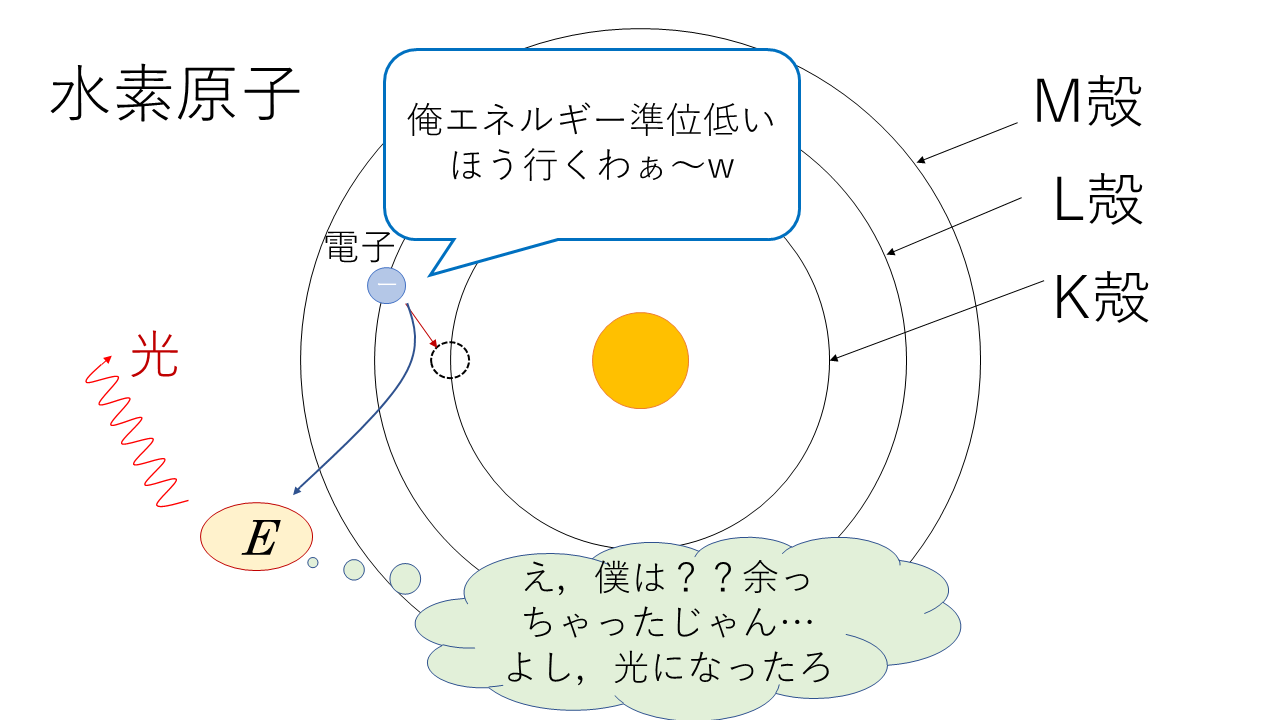
構造の一番簡単な水素での線スペクトル発生を見ていきます.
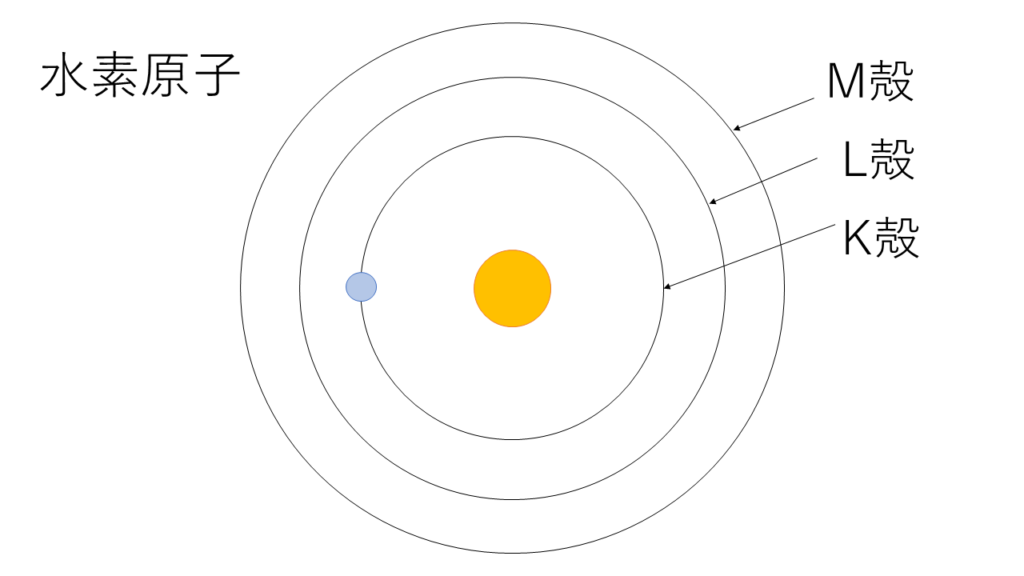
水素原子の構造はざっくりこんな感じなのは大丈夫だと思います.
ここで重要な用語の登場.
実は原子内の電子は飛び飛びの決まったエネルギーを持っているのですが,原因は電子の軌道によって電子が持っているエネルギーの大きさが決まっているからです.この電子が持つ飛び飛びのエネルギーのことを「エネルギー準位」と呼びます.結構この後も頻繁に出てくるので覚えてください.詳しくはコチラ
さっきの通り,外側の軌道にいる電子のほうが高いエネルギーを持ちます(=エネルギー準位が高い).物体は常にエネルギーの低い場所(エネルギー準位の低い軌道)を目指すので,電子はなるべくエネルギー準位の低い内側の殻に行きたがります.
通常の状態では,電子は一番エネルギー準位の低いK殻にしか入っていません.すべての電子がエネルギー準位の一番低い場所に入ったこの状態を「基底状態」と呼びます.まぁ特に何もない普通の状態のことです.エネルギー準位の低い場所はすべて埋まっている状態なので,安定しています.
温度が上がったりすると,電子がより高いエネルギーを持つようになります.この状態を「励起状態」と呼びます.励起された電子は,よりエネルギー準位の高い場所に入ることができるようになります.今回は励起されて電子がL殻に移った状態を想定します.
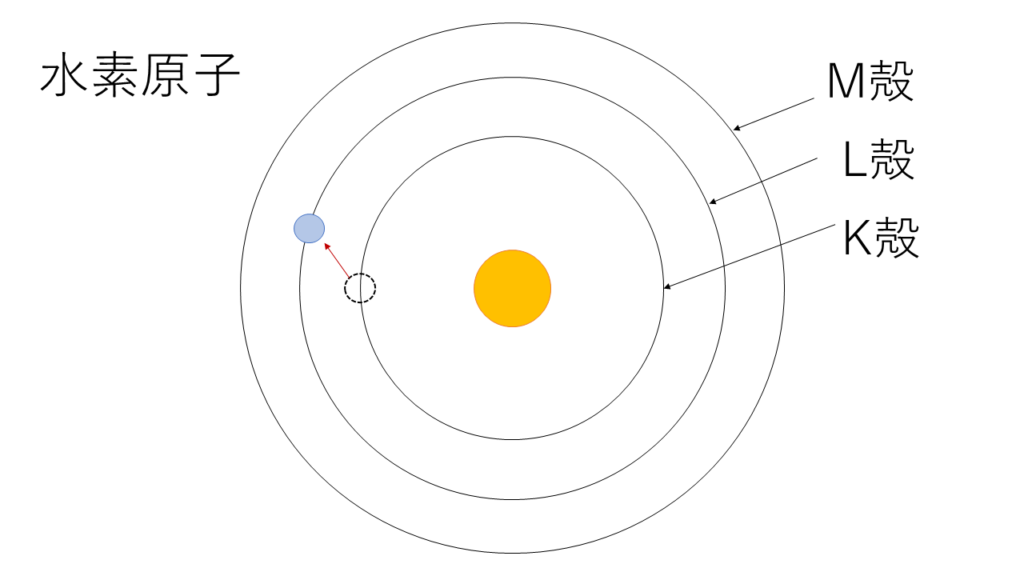
もともと基底状態で電子がいた場所が空席になりました.
自分のエネルギー準位より低い空席があれば,エネルギー準位の高い電子たちはその空席を目指します.
無事にエネルギー準位の低い状態になれた電子は,今までエネルギー準位の高い状態にあったので余分なエネルギーが発生します.この余分に余ったエネルギーが光として発生するのは先ほど説明した通りです.
例えるなら高い場所にある物体(=位置エネルギーの大きい状態)が低い場所(位置エネルギーの小さい状態)に行きたいのと同じです.物体が高いところから低い場所に移動すると,余ったエネルギーは運動エネルギーになります.線スペクトルの場合は,余ったエネルギーが光になるのです.
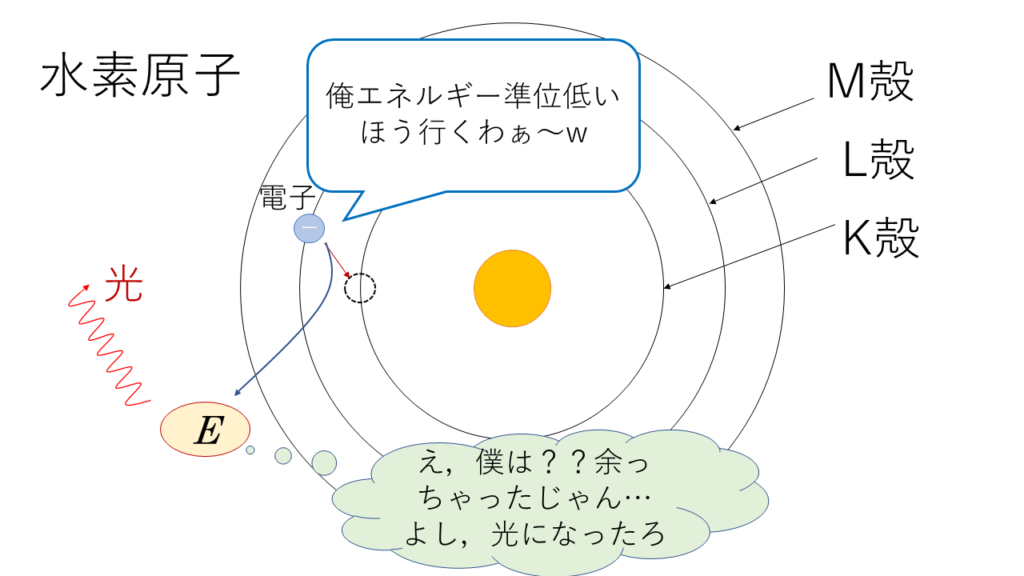
エネルギー準位はどうやって決まってるの??と思った人,鋭い!詳しくはボーアの理論でやるので今回はパス.
- 連続スペクトルと線スペクトルがある.
- 高温の気体が放つ光は線スペクトル
- 連続スペクトルの波長をもつ光を気体に当てると,その気体が高温の時出す波長の光のみ吸収する
- 線スペクトル様の波長をもつ光は,電子のエネルギー準位が下がって余ったエネルギーから発生する


コメントを残す